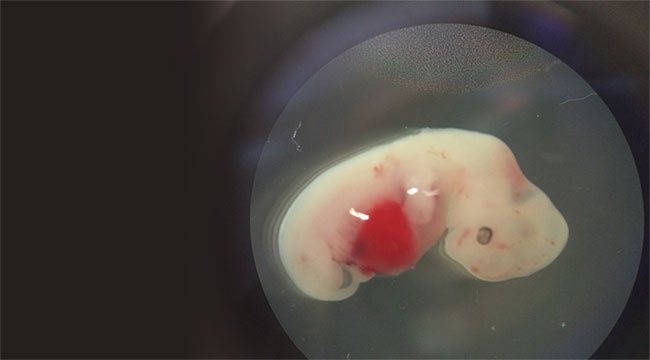
인간의 장기를 대체할 장기를 다른 동물의 몸속에서 배양하는 연구가 현실화되고 있다. 일본 도쿄대학교의 줄기세포연구소 나카우치 히로미쓰(中內啓光) 교수가 생쥐와 시궁쥐의 배아에서 인간 세포를 배양한 조직을 만들고 있기 때문이다. 국제학술지 네이처는 ‘2020년 기대할 만한 과학이슈’ 중 하나로 나카우치 교수의 이 연구를 꼽았다. ‘윤리적으로 우려되는 기법’이기도 한 이 연구의 궁극적 목적은 과연 무엇일까.
日 동물 몸속서 인간 장기 생산 연구
나카우치 교수의 연구가 주목받게 된 것은 마침내 일본 정부가 동물의 체내에서 심장 등 인간 장기를 생산하는 연구를 허용하는 새로운 법을 제정한 덕분이다.
최근 국제학술지 ‘네이처’는 일본 문부과학성 전문위원회가 인간 역분화줄기세포(iPS)를 쥐 배아에 넣어 인간 췌장 세포를 만드는 실험을 승인했다고 밝혔다. 이를 통해 사람의 몸에 이식용 장기를 안정적으로 확보하는 게 궁극의 목표다. 또 신약 효과와 독성을 사전에 실험하는 것도 하나의 계획이다.
동물 체내에서 인간 장기를 생산하기 위해서는 우선 유전자 조작으로 특정 장기를 만들 수 없게 된 동물의 배아(수정란)에 세포로 분화가 가능한 인간의 iPS를 주입한다. iPS가 배아 안에서 인간의 장기로 어느 정도 성장하면, 이 ‘하이브리드 배아(인간과 동물 세포를 합한 배아)’를 다른 동물의 자궁에 다시 주입해 인간의 장기를 몸에 지닌 새끼를 낳게 한다. 줄기세포란 미성숙세포이며 이것이 성장해 세포가 되는데, 인간의 줄기세포는 어른에게서 찾아내기 어려워 실험용으로 쓰려면 대개 배아(태아 전의 상태)에서 떼어낸다.
나카우치 교수는 이미 실험용 쥐의 배아에 인간의 iPS를 주입해 14일간 성장시키는 실험에는 성공했으나 정부 규제에 막혀 더 이상의 연구는 진행하지 못했다. 2010년에는 췌장을 만들지 못하게 된 생쥐(mouse)에 시궁쥐(rat) iPS를 넣어 췌장을 배양하는 데도 성공한 바 있다.
그렇다면 일본 정부는 그동안 교수팀의 실험을 왜 승인하지 않은 것일까. 동물과 인간의 세포가 섞이다 보면 최악의 경우 인간의 뇌를 가진 동물이 태어날 수도 있다는 게 일본 정부의 우려였다. 하지만 인간에게 이식할 장기를 가진 동물을 만든다는 목적 아래 일본 정부는 인간의 뇌와 생식세포를 제외한 장기만 동물 체내에서 생성하는 방안을 허용했다. 이렇게 iPS 임상연구가 허용되자 교수팀의 분위기는 바뀌었다.
나카우치 교수팀은 올 상반기(1∼6월) 중으로 쥐 배아에서 인간 세포를 배양한 ‘하이브리드 배아’를 만들어 대리 동물에게 이식하는 실험을 추진할 예정이다. 생쥐 유전자를 조작해 특정 장기가 없는, 즉 췌장이 없는 쥐 배아를 만든 뒤 여기에 인간 iPS를 넣을 계획이다. 이때 생쥐 배아에서 iPS는 췌장으로 성장하게 된다. 이 배아를 시궁쥐 자궁에 착상시킨 뒤 분만까지 성공한다면 사람 췌장 세포를 갖고 있는 쥐가 태어나는 세계 최초의 사례가 된다.
인간의 세포를 가진 쥐의 탄생, 즉 인간 장기를 동물 몸에서 배양한 뒤 궁극적으로 인간 몸에 이식하는 기술이 첫발을 떼는 셈이다. 네이처는 이렇게 새롭게 태어난 쥐를 ‘휴마이스’라고 이름 붙였다. 영어로 사람을 뜻하는 ‘휴먼(human)’과 복수의 쥐를 뜻하는 ‘마이스(mice)’를 합친 말이다.
지금까지 인간과 동물 세포를 결합하는 하이브리드 연구는 주로 돼지가 대상이었다. 인간의 장기와 크기가 비슷한 돼지의 장기는 이식에 안성맞춤이기 때문이다. 다만 실험 결과를 검증하기까지 시간이 너무 오래 걸린다는 게 단점으로 꼽혀왔다.
반면 쥐는 사람과 공통점이 많아 실험동물로 각광받는다. 쥐는 인간과 생김새가 완전히 다르지만 유전자는 99%가 같다. 쥐의 체내 구조와 면역 체계 또한 인간과 비슷하고, 쥐와 인간의 체온도 36.5도로 똑같다. 이런 이유로 신약의 효용을 확인하거나 화장품의 독성을 테스트할 때, 또 질병의 발병 이유를 세포나 유전자 수준에서 확인할 때도 쥐가 활용된다.
뿐만 아니다. 쥐는 한 세대의 수명이 2~3년에 불과해 돼지와 비교했을 때 훨씬 더 빠른 실험결과를 얻을 수 있다. ‘하이브리드 배아’를 만들어 인간의 세포를 가진 쥐를 탄생시키는 연구 검증 속도는 종전보다 4∼5배 정도 빨라질 것으로 기대된다.
나카우치 교수는 먼저 생쥐를 이용해 인간과 동물 간 혼합 배아를 배양하는 연구를 진행한 다음 돼지를 이용해 70일까지 혼합 배아를 배양하는 실험을 할 계획이다. 그는 현재 돼지 실험에 대한 신청서를 제출한 상태이다. 일본 문부과학성의 새로운 지침에는 돼지와 같은 동물에서 인간 장기를 충분히 기르는 연구를 허용하는 내용이 담겨 있다.

미니 인공장기 ‘오가노이드’도 주목
과학자들은 2000년대 후반부터 이식용 장기가 부족한 현 상황을 극복하기 위해 관련 연구를 꾸준히 해왔다. 미국 소크생물학연구소 연구진은 2017년 돼지 배아에 인간 iPS를 주입한 뒤 이를 암컷 돼지 자궁에 착상시켰고, 28일째 되던 날 돼지 배아 내부에서 iPS가 인체 근육과 여러 장기 세포의 초기 형태로 자란 것을 확인한 바 있다.
하지만 인간과 돼지라는 서로 다른 종의 세포가 섞인 배아는 시간이 지날수록 잘 자라지 못했다. 특히 영장류인 인간 배아는 이종 세포와 만났을 때 어울리지 못하고 죽어 버리는 게 다반사다. 그럼에도 불구하고 지금까지는 윤리 문제에 부딪혀 혼합 배아가 자라는 과정을 오랜 기간 관찰할 수 없었다. 2015년 미국국립보건원(NIH)이 인간 iPS를 비인간 척추동물의 초기 배아에 투입하는 연구비 심사를 중지한 이유이기도 하다.
나카우치 교수의 이번 연구 또한 이식용 장기 부족을 해결하는 새로운 방안이 될 수 있다는 점에서 과학기술계에의 기대감이 매우 크다. 반면 동물과 인간 세포를 융합한다는 점에서 윤리 문제에 대한 우려가 동시에 나오고 있는 게 사실이다.
이에 대해 일부 연구자들은 실험실에서 오가노이드(organoid)를 배양하는 게 더 안전하고 효율적이라고 생각하고 있다. 오가노이드는 사람이나 동물 세포, 성체줄기세포를 이용해 배양접시에서 키운 일종의 ‘미니 인공장기’이다. 따라서 윤리 문제에서 벗어날 수 있고, 실험동물의 희생도 줄일 수 있다. 세포와 달리 3차원 구조여서 진짜 장기와 더 닮은 게 장점이다.
미니 인공장기는 동물실험보다 신약 반응과 효과, 부작용을 시험하는 데 정확도가 더 높다. 현재 네덜란드왕립과학원과 위트레흐트대 의대가 설립한 휘브레흐트 오가노이드 테크놀러지(HUB)는 낭포성 섬유증 환자의 오가노이드로 약효를 시험하고 있다. 2029년쯤에는 오가노이드를 활용한 재생의학이 결실을 맺을 것이라는 게 과학자들의 설명이다.
